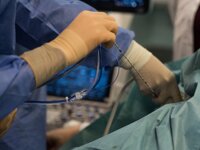
МЕТОД ТЕРМОАБЛЯЦИИ ПРИ ЛЕЧЕНИИ МЕТАСТАТИЧЕСКОГО КОЛОРЕКТАЛЬНОГО РАКА ПЕЧЕНИ
ОБЩИЕ СВЕДЕНИЯ
Колоректальный рак — это онкологическое заболевание, характеризующееся высокой распространенностью процесса. Основной причиной смерти онкологических больных, страдающих колоректальным раком, являются метастазы, и печь является главной мишенью для распространения вторичных узлов колоректального рака1. Согласно данным статистики метастазы колоректального рака в печени возникают у 20 - 25% пациентов, при этом метахронные метастазы в печени наблюдаются у других 20 – 25% пациентов с колоректальным раком2. Таким образом, метастазы в печени возникают более чем у 50% пациентов с колоректальным раком и являются основной причиной смерти этой категории больных3.
Медиана выживаемости пациентов без лечения не превышает 5 месяцев. Применение современных схем химиотерапии, в том числе с использованием таргетных препаратов, позволяет продлить жизнь пациентов с метастатическим раком печени и достичь медианы выживаемости в 2 года, однако, показатель 5-летней выживаемости составляет 0%3. Единственным радикальным методом лечения вторичных узлов колоректального рака печени является оперативное вмешательство – гепатэктомия, позволяющая добиться 5-летей и 10-летей выживаемости в 58% и 28% случаев, соответственно3. Однако, радикальное хирургическое лечение возможно не более чем в 10 – 20% случаев4, при этом послеоперационная летальность достигает 5%3.
Последние годы активно внедряются и широко используются технологии локальной терапии (абляции) метастазов колоректального рака в печени. В настоящее время существуют несколько технологий абляции печени с использованием различных видов энергии. К этим технологиям относятся радиочастотная абляция (РЧА и МВА), лазерная абляция, ультразвуковая абляция (HIFU или ФУЗ-абляция), необратимая электропорация (Nano-Knife или Нано-Нож) и криоабляция (криодеструкция). Однако только 3 технологии в 2016 году были включены в клинические рекомендации Европейского сообщества медицинской онкологии ESMO по лечению метастатического колоректального рака – это радиочастотная абляция, микроволновая абляция и криоабляция.
| Определение локализации опухолевого узла при ультразвуковом сканировании | Аппликатор для абляции излучает радиочастотное излучение на кончике |
| Введение аппликатора для абляции в опухолевую ткань через кожный прокол | Определение точности установки аппликатора опухоли |
| Запуск процесса абляции – радиочастотная энергия доставляется на кончик аппликатора по специальному защищенному кабелю | Непрерывный мониторинг процесса термоабляции печени в режиме реального времени |
В зависимости от локализации опухоли и тактики лечения, термоабляция метастазов печени может быть выполнена любым доступом открытым, лапароскопическим или чрескожным с использованием тех или иных лучевых методов визуализации тканей. Чрескожный доступ является наименее травматичным для организма, поскольку выполняется без хирургических разрезов. Открытый и лапароскопический доступ, как правило, используется при комбинированном лечении с хирургической резекцией. Какой из доступов будет предпочтительным для конкретного пациента определяется исходя из размеров опухоли, количества опухолевых узлов, локализации и общего состояния здоровья пациента.
При чрескожной абляции печени один или несколько специальный аппликаторов игольчатого типа вводятся в опухолевую ткань через кожу, не прибегая к хирургическим разрезам, как при лапароскопической или открытой абляции. Установленный в опухолевую ткань аппликатор выполняет функцию антенны, излучающей на кончике радиочастотное излучение в диапазоне ультравысоких частот на весь объем опухолевой ткани. Под действием радиочастотного излучения ткани нагреваются до крайне высоких температур, превышающих 150°С. Под воздействием таких экстремально высоких температур происходит мгновенная денатурация белка, характеризующаяся прогрессирующим коагуляционным некрозом тканей, омертвляющим раковые клетки5. Важно отметить, что радиочастотная абляция имеет направленное локальное воздействие исключительно на опухолевую ткань, поэтому окружающие ее здоровые соседние структуры и ткани не подвергаются термическому повреждению. После проведения термоабляции на месте опухоли остается мертвая и нежизнеспособная ткань, которую с течением времени организм будет естественным образом абсорбировать и замещать соединительной тканью, то есть на месте опухоли будет сформирован рубец. При определенном расположении опухолевых узлов термоабляция метастазов печени может быть выполнена под легкой седацией, но даже в этом случае может быть выбран и общий наркоз для достижения наилучших результатов лечения. В большинстве случаев после абляции печени пациент сможете вернуться домой на следующий день после вмешательства, в зависимости от общего состояния здоровья. При чрескожном выполнении абляции на коже остаются лишь крошечные проколы в местах введения аппликаторов, которое со временем полностью исчезают.
ОБЩИЕ ПОКАЗАНИЯ К АБЛЯЦИИ ПЕЧЕНИ
- Неоперабельный метастатический колоректальный рак печени
- Противопоказания к трансплантации печени
- Одиночные опухоли диаметром до 5 и более см или множественные опухоли диаметром до 4 см
- Отсутствие эффективности других методов лечения
- Рецидив опухоли после хирургического лечения
- Адекватная функция печени
- Отсутствие значимой коагулопатии
- Отсутствие венозного тромбоза
- Цирроз печени класса Child-Pugh A и Child-Pugh B
ЭФФЕКТИВНОСТЬ
Термоабляция узлов метастатического колоректального рака печени позволяет добиться 5-летней выживаемости на уровне 14 – 55% в зависимости от распространенности процесса6-8. Самые лучшие показатели 5-летней выживаемости наблюдаются при лечении солитарных метастазов диаметром до 3 см.
| Два метастатический образований колоректального рака в печени до лечения при КТ-сканировании | Два метастатический образований печени спустя 3 месяца после абляции при КТ-сканировании - полный некроз опухолей без признаков роста |
Рассмотрим более подробно эффективность внутритканевой абляции метастазов печени. Достоверность данных будет подкреплена ссылками на источники, из которых была взята та или иная информацию.
Как было показано ранее в разделе Общие сведения радикальное хирургическое лечение метастатического колоректального рака печени возможно лишь в 10 – 20% случаев5, обеспечивающее 5-летнюю выживаемость на уроне 58%3. Этот показатель несколько лучше результатов термоабляции, но не существенно, ведь разница составляет всего 3%. Принимая во внимание тот факт, что без лечения средняя продолжительность жизни пациентов с метастатическим колоректальным раком не превышает и 5 месяцев, а современные схемы химиотерапии позволяют достичь медианы выживаемости в 2 года, при этом 5-летняя выживаемость при химиотерапии составляет 0%3, то абляция является высокоэффективной альтернативой для пациентов с нерезектабельными опухолями печени метастатического колоректального рака.
В 2015 году опубликован анализ 15 научных работ по радиочастотной абляции нерезектабельных метастазов в печени открытым, лапароскопическим и чрескожным доступом14. Всего абляция была выполнена 1 613 пациентам со средним числом метастаз 2,2 (1,0 – 3,5) и средним диаметром 2,6 см (1,7 – 4,0). Средние показатели общей 3- и 5-летней выживаемости после абляции составили 50% (37 - 77%) и 31% (17 – 51%), соответственно. Интересно отметить, что лучший показатель 5-летней выживаемости наблюдался у пациентов после проведения абляции чрескожным доступом, чем открытым или лапароскопическим, показатели общей 5-летней выживаемости составили 30%, 28% и 21%, соответственно. Таким образом, чрескожная абляция это не только наименее травматичный метод лечения метастазов печени, но и наиболее эффективный по сравнению с открытой или лапароскопической абляцией. Самые лучше отдаленные результаты лечения после абляции печени наблюдались у пациентов с солитарными метастазами диаметром до 3 см. Показатели общей 3- и 5-летней выживаемости составили 80% и 51%, соответственно. Авторы сделали вывод, что радиочастотная термоабляция метастазов печени является эффективным локальным методом лечения и должна применяться как обязательный компонент терапии пациентов с метастатическим колоректальным раком печени14.
В настоящее время при сравнении клинической эффективности аппаратов для радиочастотной внутритканевой термоабляции генерирующих радиочастотное излучения разной частоты (в диапазоне средних частот радиочастотного спектра (300 – 3000 кГц или в диапазоне ультравысоких частот радиочастотного спектра (300 – 3000 МГц) не выявлено статистически значимых преимуществ одной технологии над другой при условии, что максимальный размер опухоли не превышает 2,5 - 3 см15. Абляция в диапазоне ультравысоких частот радиочастотного спектра, а именно при постоянной частоте 2450 МГц позволяет создавать значительно большую зону коагуляционного некроза за более короткий промежуток времени по сравнению с абляцией в диапазоне средних частот, поэтому сверхвысокочастотная абляция обеспечивает лучшие результаты при лечении опухолей диаметром 4 см и более3.
Важно также отметить, что число серьезных осложнений после абляции значительно меньше, чем после хирургического лечения. Так после гепатэктомии серьезные осложнения наблюдаются в 18% случаев16, а после внутритканевой термоабляции всего в 2,5%2.
На основании вышеизложенного, можно сделать вывод, что внутритканевая термоабляция – это эффективный и безопасный минимально инвазивный метод лечения, значительно продлевающий жизнь онкологических пациентов с метастатическим колоректальным раком печени.
СПИСОК ИСПОЛЬЗУЕМОЙ ЛИТЕРАТУРЫ
- Jemal A, Bray F, Center M.M, Ferlay J, Ward E, Forman D. Global cancer statistics // A Cancer Journal for Clinicians // 2011 Mar-Apr; 61(2):69-90. doi: 10.3322/caac.20107; PMID: 21296855.
- Wang J, Liang P, Yu J, Yu M.A, Liu F, Cheng Z, Yu X. Clinical outcome of ultrasound-guided percutaneous microwave ablation on colorectal liver metastases // Oncology Letters // 2014 Jul; 8(1)323-326. doi: 10.3892/ol.2014.2106; PMID: 24959270.
- Балахнин П.В, Шмелев А.С, Шачинов Е.Г. Чрескожная энергетическая абляция опухолей // Журнал Практическая Онкология // 2016 // Том 17, № 3, стр. 129-153. УДК: 616-006-08.
- Manfredi S, Lepage C, Hatem C, Coatmeur O, Faivre J, Bouvier A.M. Epidemiology and management of liver metastases from colorectal cancer // Annals of Surgery // 2006 Aug; 244(2):254-9. doi:10.1097/01.sla.0000217629.94941.cf; PMID: 16858188.
- Nikfarjam M, Muralidharan V, Christophi C. Mechanisms of focal heat destruction of liver tumors // Journal of Surgical Research // 2005 Aug // 127(2):208-23. doi: 10.1016/j.jss.2005.02.009; PMID: 16083756.
- Wong S.L, Mangu P.B, Choti M.A, Crocenzi T.S, Dodd G.D. 3rd, Dorfman G.S, Eng C, Fong Y, Giusti A.F, Lu D., Marsland T.A, Michelson R, Poston G.J, Schrag D, Seidenfeld J, Benson A.B. 3rd. American Society of Clinical Oncology 2009 clinical evidence review on radiofrequency ablation of hepatic metastases from colorectal cancer // Journal of Clinical Oncology // 2010 Jan 20; 28(3):493-508. doi: 10.1200/JCO.2009.23.4450; PMID: 19841322.
- Hompes D, Prevoo W, Ruers T. Radiofrequency ablation as a treatment tool for liver metastases of colorectal origin // Cancer Imaging // 2011 Mar 24 // 11:23-30. doi: 10.1102/1470-7330.2011.0004. PMID: 21435988.
- Sag A.A, Selcukbiricik F, Mandel N.M. Evidence-based medical oncology and interventional radiology paradigms for liver-dominant colorectal cancer metastases // World Journal of Gastroenterology // 2016 Mar 21;22(11):3127-49. doi: 10.3748/wjg.v22.i11.3127. PMID: 27003990.
- Ahmed M, Brace C.L, Lee F.T. Jr, Goldberg S.N. Principles of and advances in percutaneous ablation // Radiology // 2011 Feb // 258(2)351:69. doi: 10.1148/radiol.10081634; PMID: 21273519.
- Brace C.L. Thermal Tumor Ablation in Clinical Use // Author manuscript // 2014. PMCID: PMC4226271; PMID: 25372967; doi: 10.1109/MPUL.2011.942603.
- Hinshaw J.L, Lubner M.G, Ziemlewicz T.J, Lee F.T. Jr, Brace C.L. Percutaneous tumor ablation tools: microwave,
radiofrequency, or cryoablation – what should you use and why? // Radiographics // 2014 Sep-Oct // 34(5):1344-62. doi: 10.1148/rg.345140054; PMID: 25208284. - Zivin S.P, Gaba R.C. Technical and practical considerations for device selection in locoregional ablative therapy // Seminars in Interventional Radiology // 2014 Jun // 31(2):212-24. doi: 10.1055/s-0034-1373796; PMID: 25053866.
- Lencioni R, de Baere T, Martin R.C, Nutting C.W, Narayanan G. Image-Guided Ablation of Malignant Liver
Tumors: Recommendations for Clinical Validation of Novel Thermal and Non-Thermal Technologies – A Western
Perspective // Liver Cancer // 2015 Dec // 4(4):208-14. doi: 10.1159/000367747; PMID: 26734576. - Gillams A, Goldberg N, Ahmed M, Bale R, Breen D, Callstrom M, Chen M.H, Choi B.I, de Baere T, Dupuy D, Gangi A, Gervais D, Helmberger T, Jung E.M, Lee F, Lencioni R, Liang P, Livraghi T, Lu D, Meloni F, Pereira P, Piscaglia F, Rhim H, Salem R, Sofocleous C, Solomon S.B, Soulen M, Tanaka M, Vogl T, Wood B, Solbiati L. Thermal ablation of colorectal liver metastases: a position paper by an international panel of ablation experts, The Interventional Oncology Sans Frontières meeting 2013 // European Radiology // 2015 Dec // 25(12):3438-54. doi: 10.1007/s00330-015-3779-z; PMID: 25994139.
- Poulou L.S, Botsa E, Thanou I, Ziakas P.D, Thanos L. Percutaneous microwave ablation vs radiofrequencyablation in the treatment of hepatocellular carcinoma // World Journal of Hepatology // 2015 May // 7(8):1054-1063. doi: 10.4254/wjh.v7.i8.1054; PMID: 26052394.
- Tanaka K, Shimada H, Ueda M, Matsuo K, Endo I, Sekido H, Togo S. Perioperative complications after hepatectomy with or without intra-arterial chemotherapy for bilobar colorectal cancer liver metastases // Surgery // 2006 May // 139(5):599-607. doi: 10.1016/j.surg.2005.09.023; PMID: 16701091.